Аптечные новости:
В состав нижегородской ГК Фармассоциация вошла местна Нижегородская аптечная сеть «Фармкомплект-аптека» вошла в состав нижегородской же группы компаний «Фармассоц... |
Российская фармацевтическая ассоциация (Росфарма) Была создана в 1993 году по инициативе и при непосредственном участии фармацевтических работников . В настоя... |
История фармокологии:
История создания лекарств Создание современных лекарственных средств является одним из крупнейших научных достижений XX века. Недаром ... |
История возникновения аспирина Он родился как проявление сыновней любви, чтобы потом положить начало всемирному бизнесу. Старик, больной ар... |
История фармакологии История фармакологии также же продолжительна, как и история человечества. Для облегчения страданий при забол... |
| Государственная фармакопея: вопросы соответствия времени |
| Аптечное дело - Фармацевтический рынок |
|
В условиях продолжающейся глобализации необходимость международной гармонизации подходов к стандартизации и контролю качества ЛС уже не вызывает сомнений. Именно поэтому прошедшая в Москве международная конференция «Стандартизация качества лекарственных средств. Гармонизация требований» вызвала значительный интерес российских и иностранных специалистов. Одним из важнейших вопросов, обсуждавшихся во время конференции, стал вопрос стандартизации качества ЛС в рамках национальных и международных фармакопей. В РФ действующей является «Государственная Фармакопея CCCР XI издание» - 1 и 2 тома, содержащие только общие фармакопейные статьи. Они были выпущены в 1987 г., однако издание осталось незавершенным из-за распада СССР. Многие статьи и методы фармакопеи безнадежно устарели за прошедшее время. Такие страны, как Украина, Белоруссия, Казахстан пошли по пути создания национальных фармакопей, взяв за основу Европейскую фармакопею. В РФ в настоящее время осуществляется 12 издание государственной фармакопеи. Этому событию был посвящен доклад директора Института стандартизации и контроля лекарственных средств ФГУ НЦ ЭСМП В.Л. Багировой. Подготовка нового издания Государственной Фармакопеи - многоэтапный процесс, во время которого текст документа неоднократно подвергается доработкам и рецензируется. По мнению автора, новые эффективные методы должны вводиться в практику контроля ЛС постепенно, по мере их освоения предприятиями-производителями и приобретения ими соответствующего оборудования, а также опыта его применения. Государственная фармакопея - это документ, сосредоточивший в себе многовековой опыт отечественной фармации, он должен иметь национальные особенности. Примерно третью часть от всего объема изданной 1 части фармакопеи занимают частные фармакопейные статьи на 77 субстанции входящие в Перечень жизненно-необходимых и важнейших ЛС, а также наиболее часто используемые отечественными производителями. 2 часть Государственной фармакопеи XII издания будет содержать общие статьи, физические и физико-химические, химические, общие методы анализа, фармакопейные статьи и фармако-технологические испытания. 3 часть фармакопеи будет посвящена общим статьям на лекарственные формы и средства, иммунобиологическим ЛС и препаратам крови человека и методам анализа. В 4 части предполагается рассмотреть лекарственное растительное сырье и препараты на его основе, в 5 - гомеопатические ЛС. Е.Л.Ковалева, заместитель директора Института лекарственных средств ФГУ «Научный центр экспертизы средств медицинского применения» Росздравнадзора» в своем выступлении обратилась к роли фармакопеи в вопросах стандартизации ЛС. В настоящее время в РФ действуют национальные стандарты качества ЛС, к которым относится Государственная фармакопея (ГФ), общие фармакопейные статьи (ОФС), фармакопейные статьи (ФС) и стандарты предприятий. ГФ – это основа всей национальной лекарственной стандартизации, она является инструментом реализации государственной политики в области качества ЛС, и введения стандартов, соответствующих международному уровню. С одной стороны стандарты должны сохранять стабильность требований в течение определенного периода, а с другой – не быть тормозом в процессе совершенствования подходов в оценке качества ЛС. Поскольку качество рекомендуемых к регистрации ЛС должно быть не ниже фармакопейного уровня или качества оригинального препарата, а практика инспектирования предприятий зарубежных фирм, пока не получила должного развития, Росздравнадзором рекомендуется в нормативную документацию на ЛС зарубежного производства включать показатели, которые компания производитель относит к периодическим испытаниям и исследует на каждой серии. Например, показатель микробиологической чистоты. Национальные стандарты качества ЛС отражают уровень развития экономики, науки, производства, техническую оснащенность в стране. При работе над ГФ Росздравнадзор предусматривал подготовку ОФС и ФС в соответствии с международными требованиями с учетом возможностей и интересов отечественных производителей. Страны ЕС - это страны с развитым фармацевтическим сектором, где ЛС производятся в соответствии с правилами GMP, где обязательно предусматривают валидацию всех технологических стадий производства, необходимый контроль в процессе производства. Качество ЛС там гарантируется высоким уровнем их производства. В РФ пока иная ситуация, поэтому в национальные стандарты качества включаются дополнительные требования, в ряде случаев устанавливаются более жесткие нормы. Стандартизация ЛС и оценка качества непосредственно связана с использованием стандартных образцов. Наша страна находится только в начале пути создания национальной системы стандартных образцов. В первой части ГФ 12-го издания предусмотрено использование наряду с национальными стандартными образцами, которые раньше назывались Государственные стандартные образцы, использовать стандартные образцы ЕФ, американской фармакопеи. Впервые в ГФ включена ОФС фармацевтических субстанций, в ней определены основные принципы стандартизации и оценки качества. И около 80 ФС на сами субстанции. Основные положения отраслевых стандартов 1971, 1996 гг. и отраслевой стандарт 2001 г., стандарты качества ЛС положены в основу общих требований к субстанциям. При подготовке ФС на субстанции был принят подход ЕФ, для установления подлинности рассматривается метод ИК-спектроскопии, в количественном определении, как правило, работает с точным, хотя и цитрометрическим методом, который дополняется хромотографическими методами при оценке примесей. Поэтому было предложено включать в нормативную документацию на субстанции контроль всех остаточных органических растворителей, а не только тех, которые заявляются в досье. Несмотря на то, что первая часть Государственной фармакопеи 12 издания уже вышла из печати, вокруг нее не умолкают многочисленные споры.В такой ситуации российская фармацевтическая общественность с особым вниманием обращается к зарубежному опыту. В государствах Евросоюза действует европейская Фармакопея, а также национальные фармакопеи. Деятельности Комиссии европейской Фармакопеи, осуществляющей свою деятельность в рамках Европейского директората по контролю качества лекарственных средств (EDQM), а также самой Европейской фармакопее был посвящен доклад Сюзанн Кейтель - руководителя Европейского директората по качеству медицинской продукции. В своем докладе она, в частности, заметила, что работа над ЕФ регулируется комиссией европейской фармакопеи, в которой представлены все страны-члены и наблюдатели. Комиссия проводит заседания 3 раза в год. В остальное время ее деятельностью руководит избранный президиум. В его функции входит принятие рабочей программы, определение групп экспертов, а также утверждение всех фармакопейных текстов. Каждая монография курируется специальными законодательными группами, для нее прописаны процедуры контроля, разработаны технологии разработки и пересмотра. Монографии и статьи основываются на предложениях национальной делегаций, групп экспертов, а также отдельных представителей индустрии. Решение о включении новой монографии зависит от терапевтического эффекта ЛС, широты его использования, числа стран, одобривших продукт и подтвержденного качества. Обсуждение насущных вопросов стандартизации качества ЛС, гармонизации требований к ЛС, состоявшееся в рамках конференции, без сомнения, будет способствовать более активному включению РФ в международный информационный обмен и реализации намерения стать полноправным участником ЕФ. |
| Читайте: |
|---|
Почему БАДы:
БАДы для костей - БАД МедиосояВ число самых эффективных БАДов для костей входит препарат БАД Медисоя. Данная биодобавка не является гормональным препаратом,... |
Бады VisionНе сложно найти отзывы объясняющих понятие бадов плацебо, его эффекта. Первое упоминание плацебо относят к 1875, тогда это озн... |
Биодобавки для организма за и противБиодобавки не были созданы в наше время, они появились гораздо раньше, конечно употребляли их не в виде капсул и таблеток, а в фор... |
Больному на заметку:
Каталог лекарств:
Лечение рака толстой кишки в Израиле комплексным методом Среди основных причин развития онкологии толстой кишки называют несбалансированный рацион питания, с высоким с... |
Всё о салатахСалаты нашли свое место в разных народах мира, в особенности это относится r французской кухне, поскольку... |
Рвотные и отхаркивающие средства Рвоту могут вызывать многие вещества. По механизму действия их принято разделять на две группы: 1) рвотны... |
Препараты для спорта:
Подготовительный период (базовый этап подготовки) В этот период продолжается прием витаминов, хотя целесообразно сделать 8-10-дневный перерыв в курсовом прием... |
ИММУНОКОРРЕКТИРУЮЩИЕ СРЕДСТВА Препараты этой группы не влияют прямо на процессы формирования мускулатуры при занятиях атлетической гимнаст... |
Молекулы тестостерона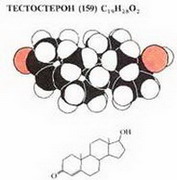 Молекулу Тестостерона можно рассматривать как укороченную молекулу холестерина (38), у которой сохранена кол... |